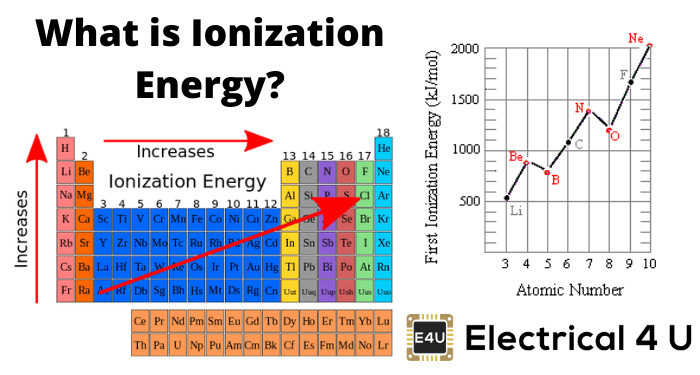
一种元素释放其最外层的电子以形成正离子的能力,表现在供应给其原子的能量足以把电子从原子中带走。这种能量被称为电离作用能量。简单地说,电离能是供应给一个孤立原子或分子的能量,它能敲除束缚最松散的价电子层电子,形成一个正离子。它的单位是电子伏的电动车或kJ/mol,在放电管中测量,在放电管中,一个快速移动的电子与一个气体元素碰撞,喷射出其中一个电子。电离能越小,形成阳离子的能力越强。

这可以用原子的玻尔模型该理论认为,在类似氢原子的原子中,电子由于哥伦布引力的作用围绕着带正电荷的原子核旋转,而电子只能有固定的或量化的能级。玻尔模型电子的能量被量子化并给出如下:
其中Z为原子序数,n为主量子数,其中n为整数。对于氢原子,电离能是13.6eV。
电离能(eV)是电子从n = 1(基态或最稳定态)到无穷大所需的能量。因此在无穷远处取0 (eV),则电离能可表示为: 电离能的概念支持玻尔原子模型的证据,电子可以围绕原子核在一个固定或离散的能级或壳层,代表的主量子数' n '。当第一个电子离开正电核附近时,当静电力吸引力增加时,移走下一个松散束缚的电子需要更大的能量,即第二个电离能比第一个电离能大。
电离能的概念支持玻尔原子模型的证据,电子可以围绕原子核在一个固定或离散的能级或壳层,代表的主量子数' n '。当第一个电子离开正电核附近时,当静电力吸引力增加时,移走下一个松散束缚的电子需要更大的能量,即第二个电离能比第一个电离能大。
例如,第一个电离能钠(Na)的浓度为:
它的第二个电离能是
因此,即2>即1(电动汽车)。这也是正确的,如果有K个离子,那么IE1<即2<即3...........<即k
金属的电离能很低。低的电离能意味着元素的导电性更好。例如,银(Ag,原子序数Z = 47)的电导率为6.30×107铜(Cu, Z = 29)的电离能为5.76×107s/m,电离能为7.726 eV。在导体低的电离能使电子在带正电的晶格中移动,形成电子云。
影响电离能的因素
在周期表中,电离能的总体趋势是从左到右增加,从上到下减少。因此,影响电离能的因素可以总结如下:
- 原子的大小:电离能随原子大小而减小,因为随着原子半径的增大,原子核与最外层电子之间的哥伦布引力减小,反之亦然。
- 屏蔽效应:内层电子的存在屏蔽或减弱了原子核与价电子之间的哥伦引力。因此电离能减少。内部电子的数量意味着更多的屏蔽。然而,在金的例子中,电离能比银大,即使金的尺寸比银大。这是因为在金的情况下,内部的d和f轨道提供了较弱的屏蔽作用。
- 核电荷:原子核的电荷越多,由于原子核和电子之间的引力越大,原子就越难以电离。
- 电子配置:原子的电子排布越稳定,就越难收回一个电子,从而获得更多的电离能。





对我的考试非常有用…Tq
别担心,Bhuvana。祝你考试好运!